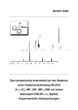
Zusammenfassung:
Die systematische Untersuchung nukleophiler
Additionen von lithiierten Organometallreagenzien bzw.
Grignardreagenzien an Carbonylverbindungen RC(O)X mit
verschiedenen Substituenten des Typs X = Aryl,
CF<SUB>3</SUB>,
NR'<SUB>2</SUB>, OR', SR' in
NMR-Tieftemperaturmessungen geben Auskunft über die Reaktivität
der eingesetzten Carbonylverbindungen und die Stabilität der
gebildeten tetraedrischen Intermediate. Hierbei konnten
eindeutige Gesetzmäßigkeiten der Abgangsgruppenqualitäten der
unterschiedlichen Substituenten im Intermediat beim Zerfall
gezeigt werden und die Stabilisierung der jeweiligen
Intermediate durch
CF<SUB>3</SUB>-Gruppen. Außerdem
wurden die Vor- und Nachteile von starken und schwachen
Nukleophilen diskutiert. <br /><br
/> Besonderes Augenmerk wurde auf das sogenannte
Weinrebamid gerichtet, ein Carbonsäureamid mit einer
N-Methyl-N-methoxy-Gruppe, das sich durch eine relativ hohe
Reaktivität gegenüber nukleophilem Angriff auszeichnet und ein
stabiles Intermediat bildet, das für synthetische Zwecke von
Nutzen ist. Andere, im Intermediat möglicherweise
chelatisierungsfähige Carbonsäureamide, ähnlich dem
Weinrebamid, bilden ebenfalls stabile Intermediate, erwiesen
sich aber nicht als so reaktiv, während Benzoylderivate mit
Pyridylresten außerordentlich reaktiv sind und sogar im Fall
des N-Pyridylrests kein stabiles Intermediatbilden. <br
/><br /> Offensichtlich spielt die
Absenkung der Aktivierungsenergie durch reaktivitätserhöhende
Chelatisierung im Übergangszustand eine entscheidende Rolle bei
der Ketonsynthese und nicht unbedingt die Stabilität des
gebildeten Intermediats.